Oktaan
|
Algemeen | |
|---|---|
| Naam | Oktaan |
| IUSTC-naam | Oktaan[1] |
| Chemiese formule | C8H18 |
| Molêre massa | 114,232 g•mol-1 |
| CAS-nommer | 111-65-9 |
| Voorkoms | Kleurlose vloeistof |
| Reuk | petrolagtig[2] |
| Fasegedrag | |
| Smeltpunt | -57,1 tot -56,6 °C |
| Kookpunt | 125,1 tot 126,1 °C |
| Digtheid | 0,703 g•cm-3 |
| Oplosbaarheid | 0,007 mg•dm-3 (teen 20 °C) |
| Viskositeit | 0,542 mPa•s (teen 20 °C)[3] |
| Termodinamies | |
| ΔfHɵ | −252,1 kJ•mol-1 |
| ΔcHɵ | −4530 kJ•mol-1 |
| Henry se konstante | 29 nmol•Pa-1•kg-1 |
| Warmtekapasiteit | 225,68 J•K-1•mol-1 |
|
Suur-basis eienskappe | |
| pKa | |
|
Veiligheid | |
| Flitspunt | 13 °C |
| Selfontbrandingspunt | 220 °C |
| LD50 | 428 mg•kg-1 (oraal, muis) |
|
Tensy anders vermeld is alle data vir standaardtemperatuur en -druk toestande. | |
| Portaal | |
- Hierdie bladsy handel oor die chemiese verbinding. Vir die petrolgraderingstelsel, sien Oktaangetal en Petrol.
Oktaan is 'n koolwaterstof en 'n alkaan met die chemiese formule C8H18, en die struktuurformule CH3(CH2)6CH3. Oktaan het 18 strukturele isomere wat verskil deur die hoeveelheid en ligging van vertakking in die koolstofketting. Een van hierdie isomere, 2,2,4-trimetielpentaan (algemeen iso-oktaan genoem), word gebruik as een van die standaardwaardes in die oktaangetal.
Oktaan is 'n komponent van petrol. Soos met alle koolwaterstowwe met lae molekulêre gewig, is oktaan vlugtig en baie vlambaar.
Voorkoms in die natuur en sintese
[wysig | wysig bron]Oktaan is 'n natuurlike bestanddeel van die grootste paraffienfraksie van ruolie en word ook in natuurlike gas aangetref.[4] Oktaan kan bv. deur middel van 'n multi-stap reaksie vanaf furfuraal gesintetiseer word.[5]

Gebruik van die term in petrol
[wysig | wysig bron]"Oktaan" word in die algemeen gebruik as 'n kort vorm van "oktaangetal", veral in die uitdrukking "hoë oktaan". Die "oktaangradering" is 'n indeks van die vermoë van 'n brandstof om die motorklap teen hoë kompressie te weerstaan, wat kenmerkend is van oktaan se vertakte ketting-isomere, veral iso-oktaan.
Die oktaangetal is oorspronklik bepaal deur brandstof uit slegs heptaan en 2,2,4-trimetielpentaan ('n hoogsvertakte oktaan) te meng en antiklopwaardes van nul aan suiwer heptaan en 100 aan suiwer 2,2,4-trimetielpentaan toe te ken. Die antiklopgradering van hierdie mengsel sal dieselfde wees as die persentasie 2,2,4-trimetielpentaan in die mengsel. Verskillende isomere van oktaan kan bydra tot 'n laer of hoër oktaangradering. Byvoorbeeld, n-oktaan (die reguit ketting van agt koolstofatome sonder vertakking) het 'n -20 (negatiewe) navorsingsoktaangradering, terwyl suiwer 2,2,4-trimetielpentaan 'n navorsingsoktaangradering van 100 het. Sommige brandstowwe het 'n oktaan hoër as 100, veral dié wat metanol, etanol of tetra-etiellood bevat.[6]
Isomere
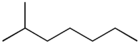
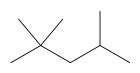
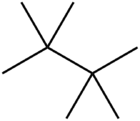
[wysig | wysig bron]Oktaan het 18 strukturele isomere (24 insluitend stereoisomere):
| Geen syketting | Een syketting | Twee sykettings | Drie sykettings | Vier sykettings |
|---|---|---|---|---|
|
|
|
|
|
*(iso-oktaan)
Verwysings
[wysig | wysig bron]- ↑ "octane - Compound Summary". PubChem Compound (in Engels). USA: National Center for Biotechnology Information. 16 September 2004. Identification and Related Records. Besoek op 17 Junie 2021.
- ↑ "NIOSH Pocket Guide to Chemical Hazards - Octane". CDC (in Engels). 30 Oktober 2019. Besoek op 17 Junie 2021.
- ↑ Dymond, J. H.; Oye, H. A. (1994). "Viscosity of Selected Liquid n‐Alkanes". Journal of Physical and Chemical Reference Data (in Engels). 23 (1): 41–53. doi:10.1063/1.555943. ISSN 0047-2689.
- ↑ Clough, S.R. (2014). "Octane". In Wexler, Philip (red.). Encyclopedia of toxicology (in Engels). London, England: Elsevier, Academic Press. pp. 652–654. doi:10.1016/b978-0-12-386454-3.00416-4. ISBN 978-0-12-386455-0. OCLC 878141491.
- ↑ Malinowski, Artur; Wardzińska, Dorota (2012). "Catalytic conversion of furfural towards fuel biocomponents". Chemik (in Engels) (66): 982–990.
- ↑ "Octane Number". Petroleum Equipment Institute (in Engels). Besoek op 17 Junie 2021.