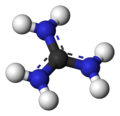
Gvanidin
| Guanidine | |||
|---|---|---|---|

| |||

| |||
| IUPAC ime |
| ||
| Identifikacija | |||
| CAS registarski broj | 113-00-8 | ||
| PubChem[1][2] | 3520 | ||
| ChemSpider[3] | 3400 | ||
| UNII | JU58VJ6Y3B | ||
| ChEMBL[4] | CHEMBL821 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | CH5N3 | ||
| Molarna masa | 59.07 g/mol | ||
| Tačka topljenja |
50 °C | ||
| pKa | 13.6 (gvanidinijum katjon)[5] | ||
| Opasnost | |||
| EU-indeks | nije na listi | ||
| Srodna jedinjenja | |||
| Srodna jedinjenja | Gvanidinijum hlorid Nitrogvanidin | ||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
Gvanidin jekristalno jedinjenje jake alkalnosti formirano oksidacijom gvanina. Ovo jedinjenje se koristi u proizvodnji plastike i eksploziva. On je sastojak urina, kao normalni proizvod proteinskog metabolizma. Molekul je bio privi put sintetisan 1861, oksidativnom degradacijom jednog aromatičnog prirodnog proizvoda, guanina, izolovanog iz peruvijskog gvana.[6] Uprkos jednostavnosti molekula, kristalna struktura je opisana tek 148 godina kasnije.[7]

Gvanidin je protonovan u fiziološkim uslovima. Konjugovana kiselina se zove gvanidinijum katjon, [CH6N3]+. Gvanidinijum katjon ima naelektrisanje od +1. Ovaj katjon je veoma stabilan u vodenim rastvorima usled efikasne rezonantne stabilizacije naelektrisanja i efikasne solvacije molekulima vode. Kao rezultat toga, njegova pKa je 13.6[5], što znači da je gvanidin veoma jaka baza u vodi.
-
model gvanidina -
kanoničke forme
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519.
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Gaulton A, Bellis LJ, Bento AP, Chambers J, Davies M, Hersey A, Light Y, McGlinchey S, Michalovich D, Al-Lazikani B, Overington JP. (2012). „ChEMBL: a large-scale bioactivity database for drug discovery”. Nucleic Acids Res 40 (Database issue): D1100-7. DOI:10.1093/nar/gkr777. PMID 21948594.
- ↑ 5,0 5,1 Perrin, D.D. (1972). Dissociation Constants of Organic Bases in Aqueous Solution. London: Butterworths. ISBN 0-08-020827-4.
- ↑ A. Strecker, Liebigs Ann. Chem. 1861, 118, 151.
- ↑ T. Yamada, X. Liu, U. Englert, H. Yamane, R. Dronskowski, Chem. Eur. J. 2009, 15, 5651.
- Perrin, D.D. (1972). Dissociation Constants of Organic Bases in Aqueous Solution. London: Butterworths. ISBN 0-08-020827-4.